بچه درس خونا!!!
سوالات درسی .بازی .آموزش و...بچه درس خونا!!!
سوالات درسی .بازی .آموزش و...جدول تناوبی عناصر چیست ؟ ( جدول تناوبی عناصر به زبان ساده )

در ادامه مطلب بیشتر با این جدول آشنا خواهید شد .
دیمیتری مندلیف شیمیدان روس معتقد بود که در عنصر ها
نظمی وجود دارد . او درباره ی همهی عنصر های
شناخته شده تا آن زمان اطلاعاتی جمع آوری کرد و در سال 1869 میلادی جدولی از عنصرها انتشار داد که
جدول تناوبی حال حاضر بر اساس آن شکل گرفته است . کار ارزشمند و مهم مندلیف در طراحی جدول این بود
که او برای عنصرهایی که پیش بینی می کرد در آینده کشف شوند ، جای خالی قرار داده بود . به عنوان مثال
یکی از عنصرهایی که مندلیف جای ان را در جدول تناوبی خالی گذاشت ، گالیم ( عنصر 31 ) بود مندلیف آن
را اکاـ آلومینیوم نامید ؛ چون پیش بینی می کرد خواص شیمیایی این عنصر مشابه آلومینیوم باشد . در سال 1875
دانشمند فرانسوی ، لوکوک دو بو ابودران ، گالیم را کشف کرد . این عنصر دقیقاً همان خواصی را داشت که
مندلیف پیش بینی می کرد .

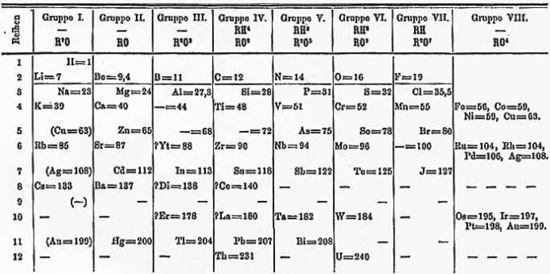
جدول طراحی شده توسط مندلیف
در نگاه نخست جدول تناوبی بسیار پیچیده به نظر می رسد . جدول تناوبی در حقیقت ، جدولی بزرگ از همه
ی عنصر های موجود است که در آن عنصر ها به ترتیب عدد اتمی ردیف شده اند . عدد اتمی ، تعداد پروتون
هایی است که هر اتم در هسته ی خود دارد . با قرار دادن عنصر ها به این شیوه ، عنصرهایی که خواص
مشابه دارند در یک گروه قرار می گیرند . مانند هر جدول دیگری ، این جدول نیز ردیف هایی دارد که از
چپ به راست و ستون هایی دارد که از بالا به پایین مرتب شده اند . ردیف های جدول تناوبی دوره تناوب و
ستون های آن گروه نامیده می شود .
هیدروژن ( H ) نخستین عنصر جدول تناوبی عناصر است ، چون فقط یک پروتون در هسته ی خود دارد .
هلیم ( He) دمین عنصر است ، چون دو پروتون دارد و سایر عنصرها نیز به همین ترتیب مرتب شده اند .
جدول تناوبی می تواند رنگ بندی شود معمولاً هر دسته ای با رنگی ویژه مشخص می شود تا تمامی
عنصرهایی که به یک دسته تعلق دارند ، به راحتی شناخته شوند . چنانچه عنصرهای جدول تناوبی رنگ بندی
شوند ، 9 دسته مختلف را نشان می دهند . هیدروژن به هیچ کدام یک از این دسته ها تعلق ندارد .

علامت اختصاری
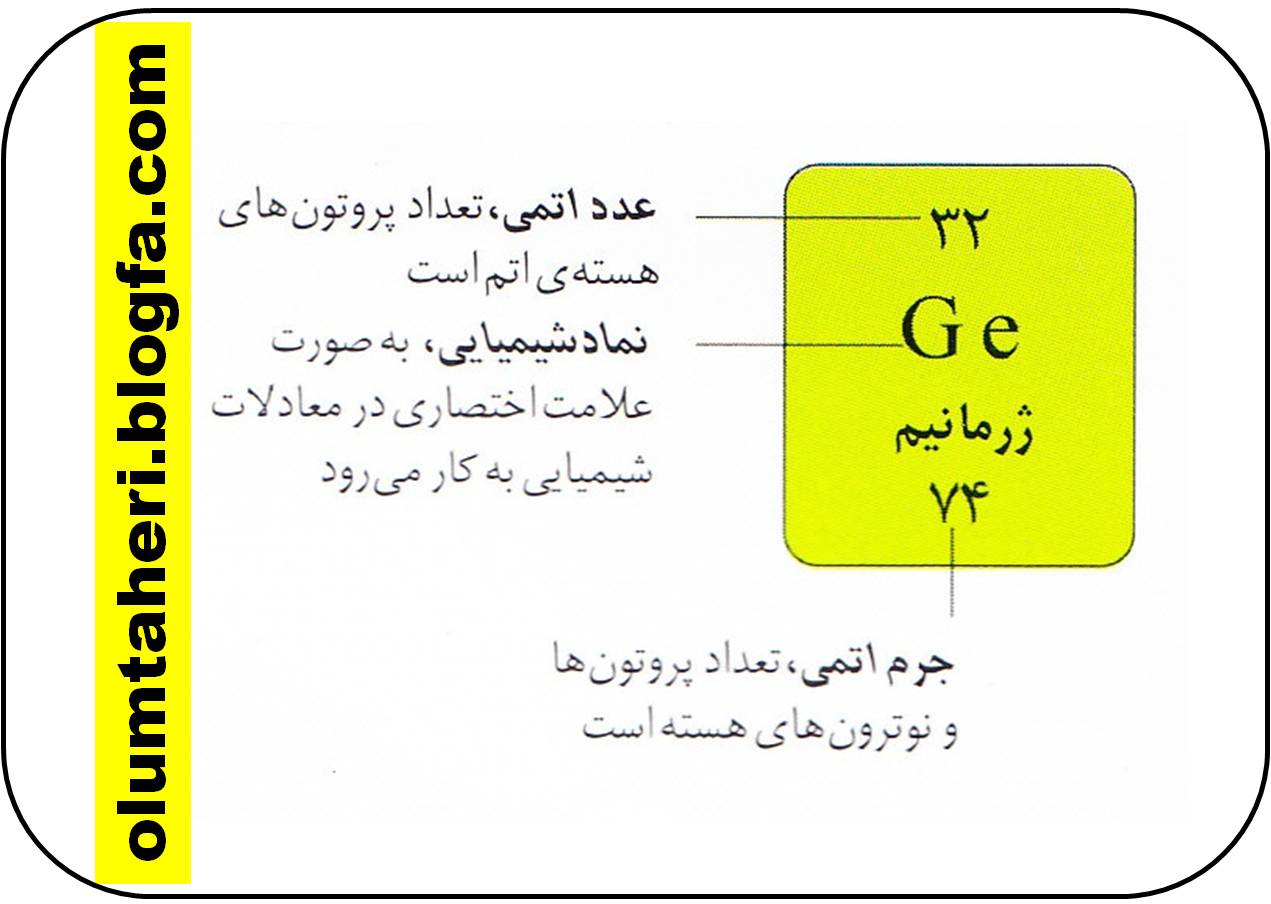
هر عنصر به غیر از نام ، یک علامت اختصاری هم دارد که به ان نماد شیمیایی گفته می شود که شیوه ی تند
نویسی عنصر در معادلات شیمیایی است . نماد شیمیایی اغلب حرف اول یا دو حرف اول اسم آن عنصر است .
هر عنصر عدد اتمی و جرمی مخصوص به خود را دارد.
گروه
جدول تناوبی 18 گروه دارد .گروه اول ( که گروه فلزات قلیایی نامیده می شود ) آخرین ستونی است که در
سمت چپ جدول قرار گرفته است . عنصرهای این گروه دارای خصوصیاتی مشابه اند ، ولی غیر یکسان
هستند . چون تعداد الکترون های لایه ظرفیت ( الکترون های آخرین لایه اتم ) در همه عناصر یک گروه
مشابه است ، اگر بدانیم یک عنصر در چه گروهی قرار دارد ، می توانیم اطلاعات زیادی راجع به آن به دست آوریم .
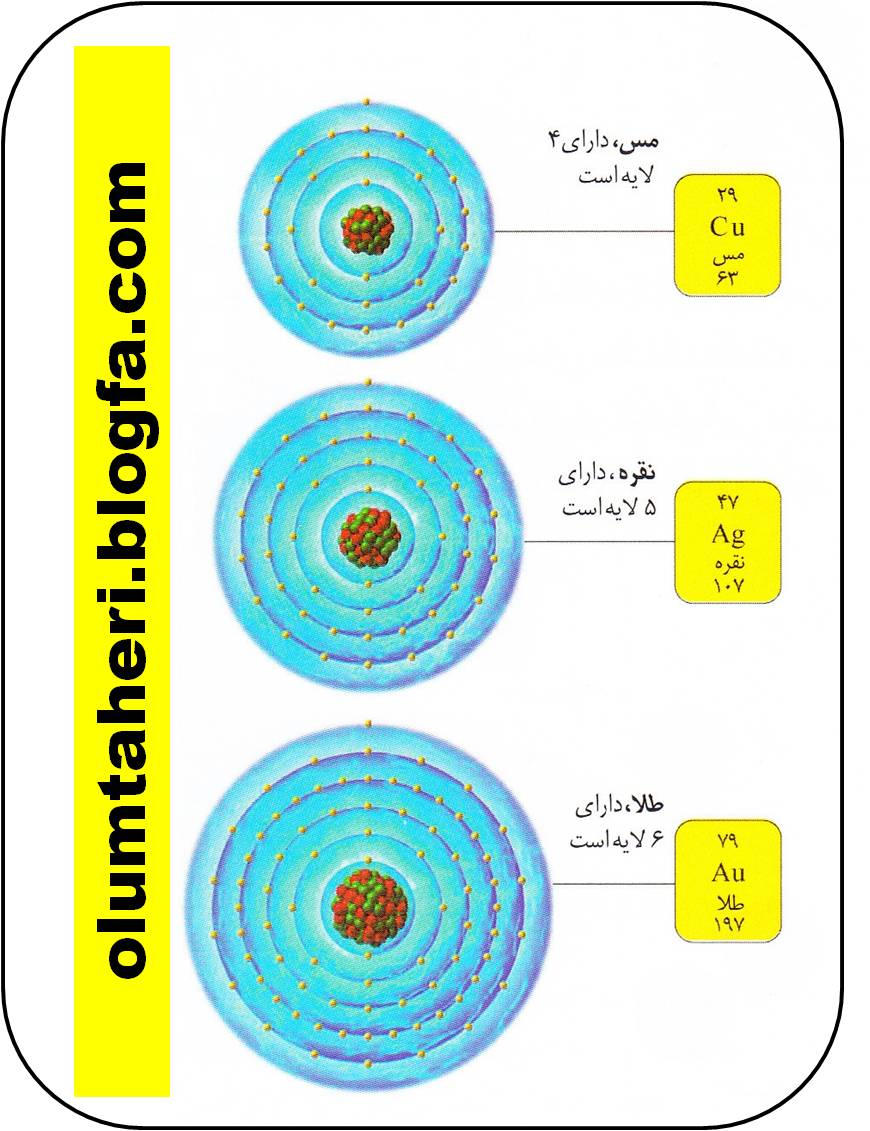
در هر گروه هر چه پایین تر برویم ، تعداد پروتون ها و نوترون ها داخل هسته افزایش می یابد و یک لایه
جدید الکترونی نیز به آن اضافه می شود . این ذرات اضافی اتم را سنگین تر می کنند و لایه اضافی حجم اتم را
بالا می برد .
برای مشاهده تصویر با کیفیت و بزرگ بالا اینجا را کلیک کنید
